Что такое миелодиспластический синдром и как его лечить
Миелодиспластический синдром относится к тяжелым патологиям системы кроветворения. Несмотря на активное развитие гематологии, лечение его очень сложное и не всегда оказывается эффективным. Прогноз выживаемости для больных зависит от степени тяжести болезни, и радикальные лечебные меры на ранней стадии становится единственным реальным шансом сохранения жизни.
Сущность патологии
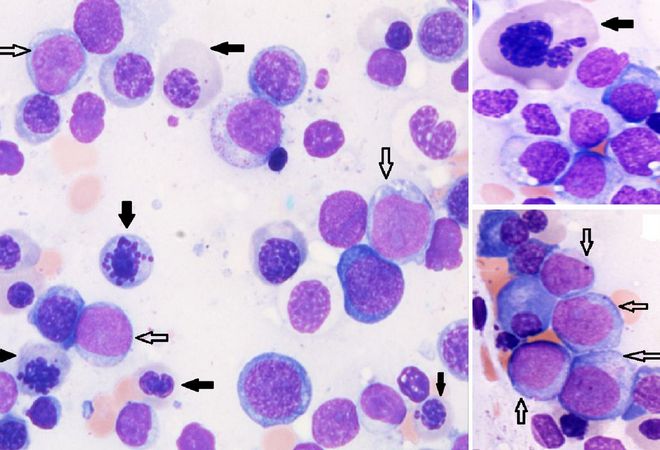
Что такое миелодиспластический синдром ( МДС )? Под этим понятием подразумевается целая группа болезней гематологического направления, связанных с нарушениями системы кровотворения миелоидной линии. Патология характеризуется изменениями костного мозга диспластического типа, наличием цитопении и повышенной вероятностью провоцирования острой формы лейкоза. Ее суть заключается в том, что, несмотря на продолжение продуцирования зрелых кровяных клеток, в организме обнаруживается нехватка некоторых видов клеток, да и сама клеточная структура претерпевает изменения, что приводит к клеточной неполноценности.
Рассматриваемый синдром не зря иногда называют «дремлющий лейкоз». У больных людей в костном мозге накапливаются бластные клетки, которые и приводят к появлению миелоидного лейкоза у большинства пациентов с указанным диагнозам.
Время до зарождения острого лейкоза колеблется от 5-6 месяцев до 8-10 лет в зависимости от тяжести течения болезни.
Миелодиспластический синдром чаще проявляется у людей старше 55-60 лет (почти 4/5 всех случаев), более подвержены болезни мужчины. В детском возрасте патология не обнаружена. Однако в последние 10-15 лет намечается определенная тенденция к омоложению среднего возраста больных, специалисты связывают это с экологией крупных городов.
Этиология явления
Этиологический механизм МДС до конца не изучен, но выявлены провоцирующие причины. Исходя из природы патологии, врачами выделяется первичный и вторичный вариант болезни. Первичный или идиопатический миелодиспластический синдром выявляется у людей старше 62-65 лет, причем причины точно не определяются, но устанавливаются факторы повышенного риска. К ним относятся: неблагоприятная экология, повышенный уровень радиации, чрезмерное курение, вредные выбросы на производстве, работа с агрессивными веществами (бензин, пестициды, растворители), наследственные патологии (болезнь Дауна, анемия Фанкони, нейрофиброматоз).
Вторичная разновидность заболевания вызывается химиотерапией, лучевой терапией и приемом некоторых сильнодействующих препаратов (Циклофосфан, подофиллотоксины, Доксорубицин, Иринотекан, Топотекан). Этот тип патологии может развиться и в молодом возрасте. Он охватывает примерно 12-18% всех выявленных случаев болезни. Прогноз выживаемости очень неблагоприятный.
Подразделение патологии
В разных странах приняты свои системы классификации МДС, что вызвано разным подходом к лечению. Часто миелодиспластические болезни классифицируются по рекомендациям ВОЗ. Исходя из этого принципа выделяются разновидности патологии:
- Анемия рефрактерного типа. Болезнь характеризуется дисплазией эритроидного ростка костного мозга при отсутствии бластных кровяных клеток. Данная форма анемии может существовать более 6 месяцев.
- Вышеуказанная анемия, но с сидеробластами кольцевого типа.
- Цитопения рефрактерного типа с дисплазией многолинейного характера. Диспластические нарушения обнаруживаются в небольшой части костномозговых клеток (не более 10 процентов). Выявляется небольшое количество бластных клеток (4-6 процентов) в костном мозге, при этом в крови бласты встречаются крайне редко. В анализе крови определяется повышенный уровень моноцитов и панцитопения.
- Анемия рефрактерного типа с высоким уровнем бластов-1. В костном мозге дисплазия охватывает несколько клеточных уровней, а концентрация бластных клеток достигают 7-10 процентов. В крови появляются бласты-1 (до 6 процентов) и большое количество моноцитов.
- То же, но с избытком бластов-2. Общее количество бластных клеток в костном мозге увеличивается до 17-20 процентов, а в крови — до 8-18 процентов. Начинают появляться тельца Ауэра, как в крови, так и в костном мозге.
- Патология , не поддающаяся классификации (МДС-Н). Дисплазия охватывает лишь один росток мегакарио- или гранулоцинарного типа. Бластные клетки в костном мозгу не превышают 4 процентов, в крови отсутствуют. В кровяном анализе наблюдается цитопения.
- Синдром, сочетающийся с 5q-делецией изолированного вида. Фиксируется кровяная анемия, иногда — тромбоцитоз. Бластные клетки превышают 6 процентов и в костном мозгу, и в крови. В костном мозге определяется 5q-делеция.
Симптоматические проявления
Симптомы рассматриваемой болезни зависят от типа патологии и степени ее тяжести. В целом, они не имеют специфического проявления, во многом похожи на признаки других заболеваний, а потому дифференцировать миелодиспластический синдром достаточно сложно. Во многих случаях начальная стадия болезни протекает со слабой выраженностью симптомов, поэтому больные не спешат к врачу, что усугубляет последующее осложнение.
Симптоматические проявления связаны с такими процессами:
- Анемия возникает при снижении уровня эритроцитов и гемоглобина. Она наиболее часто встречается при МДС. Основные признаки — бледность кожных покровов, быстрая утомляемость и общая слабость, одышка, головокружение, низкая переносимость физических нагрузок, иногда появляется болевой синдром в грудной области.
- Нейтропения обнаруживается почти у половины больных. Для нее характерно пониженное содержание полноценных, зрелых нейтрофилов. Если данный фактор преобладает в течении болезни, то повышенная температура приобретает стойкий характер. Снижается резистивность организма к инфекционным поражениям, что выражается в учащении заболеваний разного типа (простуды, стоматит, синусит и т.п.).
- Тромбоцитопения возникает при низком уровне тромбоцитов. В таком варианте появляются кровоточивость, что может выражаться кровотечениями десен и носовой полости, учащением кровотечений разного характера и появлением синяков.
- Достаточно часто (почти 25 процентов) патология приводит к увеличению лимфатических узлов, а также расширению печени и селезенки.
Диагностические мероприятия
Диагностика МДС строится на тщательном анализе периферической крови и костного мозга. Проводится общий анализ, цитологические, цитохимические и цитогенетические исследования. При исследовании крови особое внимание уделяется вычислению количества лейкоцитов, тромбоцитов и ретикулоцитов. Чаще всего у больных выявляется панцитопения, а также цитопения одного или двух ростков. В более 85 процентах случаев наблюдается анемия, а у 2/3 больных — лейкопения или нейтропения.
Характерно изменение клеточной формы, а также изменение количества ростков кроветворения.
Наиболее полную картину болезни дают результаты исследования костного мозга. Образцы его отбираются двумя основными методами — путем биопсии или трепанобиопсии из участка подвзвдошной кости. Исследования проводятся в следующих направлениях:
- Гистология костного мозга дает возможность изучить изменение строения, наличие поражения диффузного или очагового характера, установить наличие аномальных клеток, определить баланс кроветворной и жировой ткани.
- Биохимический анализ оценивает процесс обмена железа, витаминов и фолиевой кислоты.
- Иммунологические пробы и цитогенетические исследования направлены на выявление хромосомных аномалий.
Диагностические исследования должны помочь поставить точный диагноз, и только на его основании может быть начато лечение. Дифференцировать МДС необходимо от таких патологий, как анемии при дефиците витамина В12, фолиевой кислоты; анемия апластического типа; миелолейкоз и иные острые формы лейкоза; заболевания лимфопролиферического характера. Похожие симптомы могут возникать при отравлениях тяжелыми металлами.
В соответствии с международной классификацией установлены такие минимальные диагностические критерии:
- длительная, устойчивая цитопения продолжительностью не менее 5,5-6,5 месяцев;
- дисплазия, охватывающая более 8 процентов клеток в костном мозге;
- количество бластных клеток в пределах 6-18 процентов;
- появление аномального кариотипа — 5q, 20q или 7q делеции;
- дополнительное условие — обнаружение молекулярных маркеров.
Принципы лечения
При постановке точного диагноза миелодиспластического синдрома и появлении риска лейкоза обеспечивается интенсивное лечение с применением комплексной терапии, химиотерапии, иммуносупрессивных методик. При тяжелом течении болезни осуществляется трансплантация костного мозга.
Наиболее распространена комплексная, сопроводительная терапия. Она базируется на внутривенном введении кровяных ингредиентов. Для исключения избыточного повышения содержания железа при такой процедуре назначаются препараты для связывания железа (хелаторы — Десферал, Эксиджад).
Иммуносупрессорное лечение проводится в присутствии гена HLA-DR15 и костномозговых гипоклеток. Чаще всего вводится препарат Леналидомид. Химиотерапия необходима при высоком риске возникновения острой формы лейкоза; при выявлении такой разновидности МДС, как анемия с большим содержанием бластных клеток; костном мозге гиперклеточного типа. Для обеспечения лечения используется Цитарабин.
Эффективность лечения повышается при назначении гипометилирующих лекарств.
В частности, используются ингибиторы типа Азацитидина или Децитабина, иммуномодуляторы двойного воздействия.
Прогноз выживаемости больных основывается на степени тяжести патологии. С учетом этого показателя выделяется 5 категорий МДС. Наиболее легкая форма позволяет обеспечить эффективное лечение, и продолжительность жизни превышает 12-14 лет. Прогноз жизни в самой тяжелой группе не превышает 9-10 месяцев.
Миелопластический синдром является тяжелой патологией и, как правило, трансформируется в острый лейкоз. Только своевременное выявление и адекватное лечение может обеспечить максимальное продление жизни.